
Video: Hvordan påvirker absorption og frigivelse af energi temperaturændringer under en kemisk reaktion?

2024 Forfatter: Miles Stephen | [email protected]. Sidst ændret: 2023-12-15 23:34
I endotermisk reaktioner produkternes entalpi er større end reaktanternes entalpi. Fordi reaktioner frigiver eller absorbere energi , de påvirke det temperatur af deres omgivelser. Eksotermisk reaktioner opvarme deres omgivelser, mens de er endotermiske reaktioner køl dem ned.
På samme måde kan du spørge, hvordan energi frigives eller absorberes under en kemisk reaktion?
Energi og Kemiske reaktioner Energi bruges til at bryde bindinger i reaktanter, og energi frigives når nye bindinger dannes i produkter. I andre kemiske reaktioner , der skal mere til energi at bryde bindinger i reaktanter end det er frigivet når der dannes bindinger i produkter. Disse reaktioner , kaldet endotermisk reaktioner , absorbere energi.
På samme måde, hvilke energiændringer sker i kemiske reaktioner? Kemiske reaktioner ofte involverer ændringer i energi på grund af brud og dannelse af bindinger. Reaktioner i hvilken energi frigives er eksoterme reaktioner , mens dem, der tager varme energi er endoterme.
Når man tager dette i betragtning, hvordan ændres temperaturen under en kemisk reaktion?
Hvis to stoffer reagerer, og den temperatur af blandingen falder, den reaktion er endotermisk. Hvis to stoffer reagerer og temperatur af blandingen stiger, den reaktion er eksoterm. EN kemisk reaktion involverer brydning af bånd i reaktanterne og dannelsen af bindinger i produkterne.
Hvordan ændrer energi sig fra en form til en anden i en eksoterm reaktion?
An eksoterm reaktion er en der frigiver energi i form af varme eller lys. I andre reaktioner , det energi der skal absorberes for at bryde bindingerne i reaktanterne, er mere end energi at er frigives, når de nye bindinger i produkterne dannes.
Anbefalede:
Hvad er atomer ikke under en kemisk reaktion?

Atomer skabes eller ødelægges ikke under en kemisk reaktion. Forskere ved, at der skal være det SAMME antal atomer på hver side af LIGNING. For at afbalancere den kemiske ligning skal du tilføje COEFFICIENTS foran de kemiske formler i ligningen. Du kan ikke TILFØJE eller ÆNDRE abonnementer
Hvilken type organisme bruger energi fra sollys og omdanner det til kemisk energi?
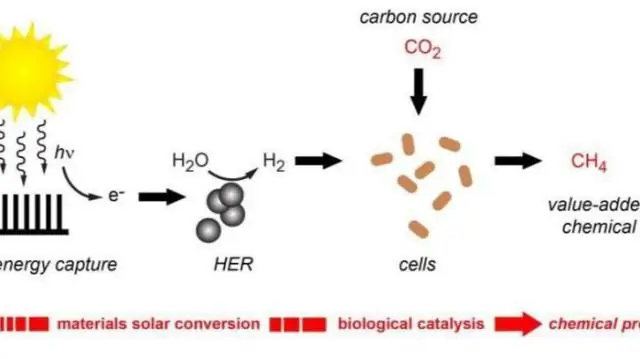
Fotosyntese er den proces, hvorved organismer, der indeholder pigmentet klorofyl, omdanner lysenergi til kemisk energi, som kan lagres i de molekylære bindinger af organiske molekyler (f.eks. sukkerarter)
Hvilke faktorer påvirker hastigheden af en kemisk reaktion?

De faktorer, der påvirker reaktionshastigheder, er: overfladeareal af en fast reaktant. koncentration eller tryk af en reaktant. temperatur. arten af reaktanterne. tilstedeværelse/fravær af en katalysator
Er kemisk energi en form for potentiel energi?

Kemisk potentiel energi er en form for potentiel energi relateret til det strukturelle arrangement af atomer eller molekyler. Dette arrangement kan være resultatet af kemiske bindinger i et molekyle eller på anden måde. Kemisk energi af et kemisk stof kan omdannes til andre former for energi ved en kemisk reaktion
Hvad er en kemisk reaktion og en fysisk reaktion?

Forskellen mellem en fysisk reaktion og en kemisk reaktion er sammensætningen. Ved en kemisk reaktion sker der en ændring i sammensætningen af de pågældende stoffer; i en fysisk ændring er der en forskel i udseendet, lugten eller simpel visning af en prøve af stof uden ændring i sammensætningen
