
Video: Hvad er hybridiseringen af i3?
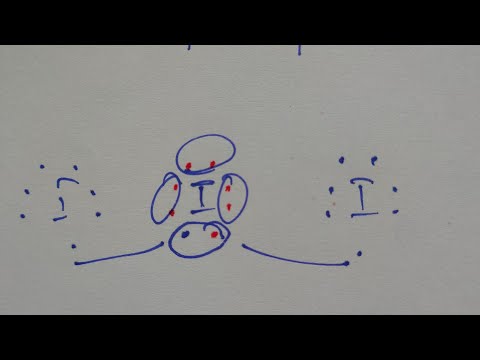
2024 Forfatter: Miles Stephen | [email protected]. Sidst ændret: 2023-12-15 23:34
Oprindeligt besvaret: Hvad er hybridiseringen af i3 ? I3 ^- har sp3d hybridisering da den har 3 enlige par og 2 bindingspar. Da de enlige par indtager ækvatorialpositionerne og bindingspar indtager aksiale positioner, er det lineært i form.
I overensstemmelse hermed, hvordan beregner du hybridisering af i3?
En anden måde at finde hybridisering af et givet molekyle er ved hjælp af enlige par og valenselektroner. Antallet af enlige par i dette molekyle er 3, og antallet af atomer, der deler valenselektroner, er 2. Derfor er 3+2=5, som også bestemmer sp3d hybridisering . Formen af et molekyle I3 - er lineær.
På samme måde, hvad er geometrien af i3 minus? Dette giver en trigonal bipyramidal form . Elektronparrene frastøder hinanden, så de ønsker at maksimere deres afstand fra hinanden, så de indtager ækvatoriale positioner 120 grader fra hinanden, og de to andre joder er 180 fra hinanden. Altså det overordnede form er lineær.
I overensstemmelse hermed, hvad er hybridiseringen af i3 negativ?
I3 - Molekylær geometri og bindingsvinkler I3 - molekylær geometri er lineær. Mens der er tre jodatomer, har et af atomerne en negativ ladning som yderligere giver 3 ensomme elektronpar og 2 bindingspar. Dets steriske tal vil være 5. De tre ensomme par vil afvise hinanden og indtage ækvatoriale positioner.
Hvad er hybridiseringen af det centrale jodatom i i3 -?
Svaret er: centralt jodatom i triiodidehas sp3d hybridisering . I triiodid anion centraliod atom har tre ækvatoriale ensomme elektronpar, og de terminale joder er bundet aksialt i en lineær form. Elektroner i sp3d hybridisering er arrangeret i trigonalbipyramidal symmetri.
Anbefalede:
Hvad er hybridiseringen af siliciumdioxid?

Silicium i silica danner 4 sigma-bindinger, så dets hybridisering er sp3
Hvad er hybridiseringen af det centrale atom i TeCl4?

Da TeCl4 har fire bindingspar og et ubundet par, er dens geometri baseret på den trigonale bipyramidale struktur. Men da der kun er fire bindingspar, antager molekylet en vippeform, og de ubundne elektroner træder i stedet for et bundet grundstof. For trigonale bipyramidale strukturer er hybridiseringen sp3d
Hvad er hybridiseringen af svovl i sf6?

Svovlatomet i svovlhexafluorid, SF6, udviser sp3d2-hybridisering. Et molekyle af svovlhexafluorid har seks bindingspar af elektroner, der forbinder seks fluoratomer til et enkelt svovlatom. Der er ingen ensomme elektronpar på det centrale atom
Hvad er hybridiseringen af C i COCl2?

Cl−(C=O)−Cl indeholder en dobbeltbinding, så den har sp2 hybridisering
Hvad er hybridiseringen af oxygenatomet?

Svar: Oxygenatomet skal have enten sp2- eller sp-hybridisering, fordi det har brug for en p-orbital for at deltage i C–O π bånd. Dette oxygenatom har tre vedhæftninger (kulstofparret og to ensomme par), så vi bruger sp2 hybridisering
