
Video: Hvordan er ladningen og massen af en proton og neutron sammenlignet?

2024 Forfatter: Miles Stephen | [email protected]. Sidst ændret: 2023-12-15 23:34
Hvordan gør opladningen og masse af en neutron sammenligne til ladning og masse af en proton ? Deres masser er næsten lige, men protoner have en positiv oplade og neutroner har en neutral oplade . Hvis du mister en elektron, så du er tilbage med mere positivt oplade end negativ oplade.
Når man holder dette for øje, hvordan er massen af en proton og en neutron sammenlignet?
Det masse af en neutron er lidt større end massen af en proton , som er 1 atomart masse enhed (amu). (Et atom masse enhed svarer til ca. 1,67×10−27 kg.) A neutron har også omtrent samme diameter som en proton , eller 1,7×10−15 meter.
På samme måde, hvad er massen af elektron og proton? Nuklear bindende energi og massedefekten
| Partikel | Masse (kg) | Masse (Mev/c2) |
|---|---|---|
| 1 atommasseenhed | 1,660540 x 10-27 kg | 931,5 MeV/c2 |
| neutron | 1,674929 x 10-27 kg | 939,57 MeV/c2 |
| proton | 1,672623 x 10-27 kg | 938,28 MeV/c2 |
| elektron | 9,109390 x 10-31 kg | 0,511 MeV/c2 |
Spørgsmålet er også, hvad er ladning og masse af proton?
EN proton er en subatomær partikel med en positiv elektrisk oplade . Protoner findes i kernen af hvert atom, men kan også findes væk fra kernen, oftest som ioniseret brint. EN proton har en oplade på +1 eller 1e, hvilket er lig med 1,602 x 10^-19 coulombs, og en masse på 1,67 x 10^-27 kg.
Hvorfor er forholdet mellem ladning og masse af en proton anderledes?
Hvorfor er oplade af masseforhold af en elektron det samme uanset den gas, der tages i et rør, mens den oplade af masseforhold er forskellige til protoner ? Så for forskellige gasser, som deres tilsvarende kerner vil have forskellige antallet af neutroner så forhold viser sig at være forskellige.
Anbefalede:
Hvordan finder man ladningen af en partikel?

I fysik er en ladet partikel en partikel med en elektrisk ladning. Det kan være en ion, såsom et molekyle eller et atom med et overskud eller underskud af elektroner i forhold til protoner. Det kan også være en elektron eller en proton eller en anden elementær partikel, som alle antages at have den samme ladning (undtagen antistof)
Hvad er forskellen mellem massen af en proton og massen af en elektron?
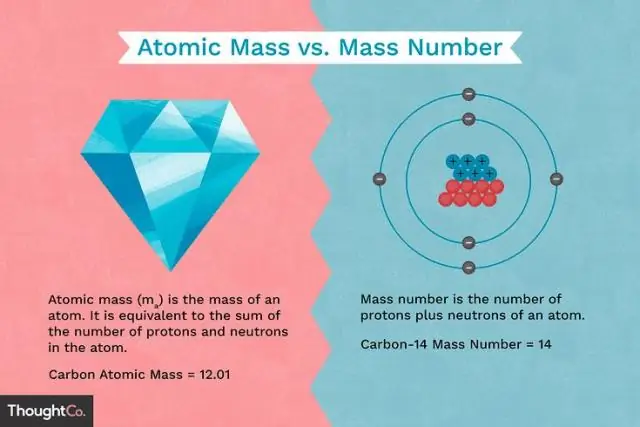
Protoner og neutroner har omtrent samme masse, men de er begge meget mere massive end elektroner (ca. 2.000 gange så massive som en elektron). Den positive ladning på en proton er lig med den negative ladning på en elektron
Hvordan er masserne af protoner og neutroner og elektroner sammenlignet?

Protoner og neutroner har meget ens masse, mens elektroner er langt lettere, cirka 11800 gange massen. Protoner er positivt ladede, neutroner har ingen elektrisk ladning, elektroner er negativt ladede. Størrelsen af ladningerne er den samme, tegnet er modsat
Hvordan er overfloden af grundstoffer på Jorden sammenlignet med overflod af grundstoffer hos mennesker?

Ilt er det mest udbredte grundstof både på Jorden og hos mennesker. Overfloden af grundstoffer, der danner organiske forbindelser, stiger hos mennesker, mens mængden af metalloider stiger på Jorden. De elementer, der er rigelige på Jorden, er afgørende for at opretholde liv
Hvordan er det genetiske materiale i hver ny celle dannet ved celledeling sammenlignet med det genetiske materiale i den oprindelige celle?

Mitose resulterer i to kerner, der er identiske med den oprindelige kerne. Så de to nye celler dannet efter celledeling har det samme genetiske materiale. Under mitosen kondenserer kromosomerne fra kromatin. Når de ses med et mikroskop, er kromosomer synlige inde i kernen
