
Video: Overtræder so3 oktetreglen?
2024 Forfatter: Miles Stephen | [email protected]. Sidst ændret: 2023-12-15 23:34
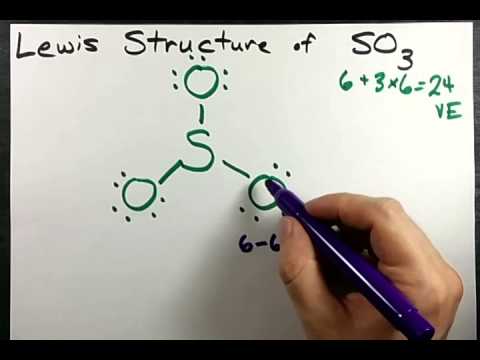
Hvorfor SO3 er stabil
Svovl danner en udvidet oktet . Det betyder, at den ikke rigtig adlyder oktet reglen , så den kan optage ekstra elektroner. Svovl er et 3. periodes grundstof; derfor kan den bruge sine 3d orbitaler til at lave mere end 4 bindinger.
Er so3 på denne måde en undtagelse fra oktetreglen?
Skulle simpelthen danne en dobbeltbinding med et hvilket som helst af oxygenatomerne. Da alle 3 bindinger i virkeligheden er lige store og symmetriske, er bindingerne hybrider af dativ enkeltbinding og (delt) dobbeltbinding.
Derudover, hvorfor overtræder svovl oktetreglen? Atomer i disse perioder kan følge efter oktet reglen , men der er forhold, hvor de kan udvide deres valenceskaller til at rumme mere end otte elektroner. Svovl og fosfor er almindelige eksempler på denne adfærd. Svovl kan Følg oktet reglen som i molekylet SF2. Hvert atom er omgivet af otte elektroner.
På samme måde, hvilke elementer kan overtræde oktetreglen?
Svovl, fosfor, silicium og klor er almindelige eksempler på elementer der danner en udvidet oktet . Phosphorpentachlorid (PCl5) og svovlhexafluorid(SF6) er eksempler på molekyler, der afviger fra oktet reglen ved at have mere end 8 elektroner omkring det centrale atom.
Overtræder PCl3 oktetreglen?
Spørgsmål: Tegn Lewis-strukturerne og bestem, hvilke af disse molekyler der har et centralt atom, der Overtræder Oktetreglen . gør Det centrale atom Overtræde Oktetreglen Eller Gør Iltatomerne? Brug formelle gebyrer til at beslutte. PCl3 BCl3 NO3- XeF2 SO2 CS2 IF5
Anbefalede:
Hvorfor overtræder BeCl2 oktetreglen?

BeCl2 overtræder oktetreglen. Boren skal være i en passende valenstilstand for at binde sig til de tre klorer. I molekylet er bor kun forbundet med seks elektroner. Meget af kemien i dette molekyle og lignende er forbundet med den resulterende stærke elektrofile natur
Hvad er gebyret for so3?

Oxidationstilstandene i SO3(g) er: Svovl (+6) & ilt (-2), fordi SO3(g) ikke har nogen ladning. I (SO3)2 - (aq) er oxidationstilstandene imidlertid: Svovl (+4) & ilt (-2). Bliv ikke forvekslet med de to, de kan begge skrives uden ladningen, men hvis SO3 er (aq) vil den have en ladning på -2
