Indholdsfortegnelse:

Video: Hvordan beregner man titreringsproblemer?

2024 Forfatter: Miles Stephen | [email protected]. Sidst ændret: 2023-12-15 23:34
Titreringsproblem Trin-for-trin løsning
- Trin 1: Bestem [OH-] Hver mol NaOH vil have et mol OH-.
- Trin 2: Bestem antallet af mol OH- Molaritet = antal mol/volumen.
- Trin 3: Bestem antallet af mol H+
- Trin 4: Bestem koncentrationen af HCl.
På samme måde kan man spørge, hvordan man beregner titrering?
Brug titrering formel. Hvis titranten og analytten har et molforhold på 1:1, er formlen molaritet (M) af syren x volumen (V) af syren = molaritet (M) af basen x volumen (V) af basen. (Molaritet er koncentrationen af en opløsning udtrykt som antallet af mol opløst stof pr. liter opløsning.)
Udover ovenstående, hvad er molariteten af NaOH? For eksempel en 0,25 M NaOH opløsning (dette læses som 0,25 molær) indeholder 0,25 mol af natriumhydroxid i hver liter opløsning. Hver gang du ser forkortelsen M, skal du straks tænke på den som mol/L.
Heraf, hvordan finder du koncentrationen af HCl fra titrering med NaOH?
Beregn koncentrationen af saltsyren
- Volumen af natriumhydroxidopløsning = 25,00 ÷ 1000 = 0,0250 dm 3
- Mængde natriumhydroxid = 0,200 × 0,0250 = 0,005 mol.
- Fra ligningen reagerer 0,005 mol NaOH med 0,005 mol HCl.
- Volumen af saltsyre = 22,70 ÷ 1000 = 0,0227 dm 3
Hvad er indikator ved titrering?
Indikator : Et stof, der skifter farve som reaktion på en kemisk ændring. En syre-base indikator (f.eks. phenolphtalein) ændrer farve afhængigt af pH. Redox indikatorer bruges også. En dråbe indikator opløsning tilsættes titrering i begyndelsen; endepunktet er nået, når farven ændres.
Anbefalede:
Hvordan beregner man standardafvigelsen fra PMP?

Formlen brugt i PMBOK for standardafvigelse er enkel. Det er bare (P-O)/6. Det er det pessimistiske aktivitetsestimat minus det optimistiske aktivitetsestimat divideret med seks. Problemet er, at denne form eller form på ingen måde giver et mål for standardafvigelse
Hvordan beregner man Jordens omkreds på dens breddegrad?

Omkredsen af en cirkel er lig med 2πr hvor r er dens radius. På Jorden er kuglens omkreds på en given breddegrad 2πr(cos θ), hvor θ er breddegraden og r er jordens radius ved ækvator
Hvordan beregner man frekvens ud fra frekvens og procent?
For at gøre dette skal du dividere frekvensen med det samlede antal resultater og gange med 100. I dette tilfælde er frekvensen af den første række 1, og det samlede antal resultater er 10. Procentdelen ville så være 10,0. Den sidste kolonne er kumulativ procentdel
Hvordan beregner man potentielt fald i et kredsløb?
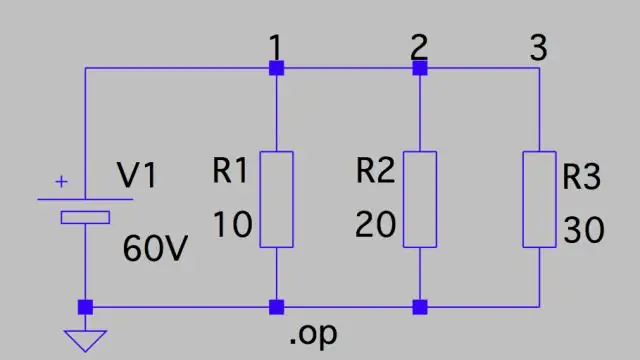
Spændingsfald: Parallel kredsløb Dette betyder, at spændingsfaldet over hver af dem kun er kredsløbets samlede spænding divideret med antallet af modstande i kredsløbet, eller 24 V/3 = 8 V
Hvordan beregner man den procentvise mængde af klor?

Klorisotopen med 18 neutroner har en overflod på 0,7577 og et massetal på 35 amu. For at beregne den gennemsnitlige atommasse skal du gange brøken med massetallet for hver isotop og derefter lægge dem sammen
