
Video: Hvad er Subshell og Orbital?
2024 Forfatter: Miles Stephen | [email protected]. Sidst ændret: 2023-12-15 23:34
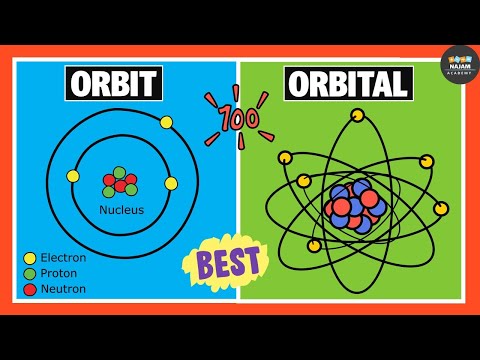
Hver subshell er yderligere opdelt i orbitaler . An orbital er defineret som et område af rummet, hvori en elektron kan findes. Kun to elektroner er mulige pr orbital . Således er s subshell kan kun indeholde én orbital og p subshell kan indeholde tre orbitaler . Hver orbital har sin egen distinkte form.
Tilsvarende, hvad er skaller underskaller og orbitaler?
Elektron skaller bestå af en eller flere underskaller , og underskaller består af et eller flere atomare orbitaler . Elektroner i samme subshell har samme energi, mens elektroner er forskellige skaller eller underskaller har forskellige energier.
Derudover, hvad er en Subshell? EN subshell er en underopdeling af elektronskaller adskilt af elektronorbitaler. Subshells er mærket s, p, d og f i en elektronkonfiguration.
Simpelthen, hvad er forskellen mellem Subshell og Orbital?
2 svar fra ekspertvejledere En shell indeholder en eller flere underskaller . EN subshell indeholder en eller flere orbitaler . An orbital kan indeholde op til 2 elektroner.
Hvor mange orbitaler er der i en underskal?
Dette fortæller os, at hver underskal har dobbelt så mange elektroner pr. orbital. s-underskallen har 1 orbital, der kan rumme op til 2 elektroner, p-underskallen har 3 orbitaler der kan rumme op til 6 elektroner, har d subshell 5 orbitaler der rummer op til 10 elektroner, og f-underskallen har 7 orbitaler med 14 elektroner.
Anbefalede:
Hvad er orbital med lavest energi?

På det laveste energiniveau, det tættest på atomcentret, er der en enkelt 1s orbital, der kan rumme 2 elektroner. På det næste energiniveau er der fire orbitaler; en 2s, 2p1, 2p2 og en 2p3. Hver af disse orbitaler kan indeholde 2 elektroner, så i alt 8 elektroner kan findes på dette energiniveau
Hvor mange noder er der i en antibonding orbital?

Hver orbital indeholder to elektroner. π4 ogπ5 er degenererede antibindings-orbitaler med to noder i rette vinkler på hinanden. π6 er en antibindende orbital med tre noder
Hvilken d orbital er involveret i sp3d2 hybridisering?

Hvilke d orbitaler er involveret i henholdsvis sp3d2 og d2sp3 hybridisering? Svar:sp3d2 ord2sp3 er hybridisering for teoktaedrisk geometri. I oktaeder dannes bindingerne parallelt med x-, y- og z-akserne, derfor vil dx2-dy2 ogdz2 blive brugt til at danne hybridorbitaler
Hvad er Orbital i kemi?

Orbital definition. I kemi og kvantemekanik er en orbital en matematisk funktion, der beskriver den bølgelignende opførsel af en elektron, elektronpar eller (mindre almindeligt) nukleoner. En orbital kan indeholde to elektroner med parrede spin og er ofte forbundet med en specifik region af et atom
Hvad er en orbital i det periodiske system?

Værktøj: Interaktivt periodisk system. Orbitaler og elektroner. En orbital er et område med sandsynlighed, hvor elektronen kan findes. Disse områder har meget specifikke former, baseret på energien fra de elektroner, der vil optage dem
