
Video: Hvorfor har vand et højt kogepunkt og smeltepunkt?

2024 Forfatter: Miles Stephen | [email protected]. Sidst ændret: 2023-12-15 23:34
Årsagen til høj smeltning og kogetemperaturer er hydrogenbindingen mellem vand molekyler, der får dem til at klæbe sammen og modstå at blive trukket fra hinanden, hvilket er det, der sker, når is smelter og vand koger til at blive en gas.
Desuden, hvorfor er det vigtigt, at vand har et højere kogepunkt?
Vand har stærke hydrogenbindinger mellem molekyler. Disse bindinger kræver meget energi, før de går i stykker. Dette fører til vand have en højere kogepunkt end hvis der kun var svagere dipol-dipolkræfter. Vand er i stand til at absorbere infrarød stråling (varme) fra solen.
Desuden, hvad er højt smelte- og kogepunkt? Metaller har højest kogende og smeltepunkter fordi de har de stærkeste kemiske bindinger som er metalliske. De fleste af metallerne er til stede i fast tilstand i normalt rum temperatur . Dette skyldes, at molekylerne holdes sammen af en stærk molekylær kraft af metallisk binding til at danne en hård gitterstruktur.
I betragtning af dette, har vand et højt eller lavt smeltepunkt?
Vand molekyler er knyttet til hinanden ved hjælp af hydrogenbindinger, som er lidt stærkere end van dar Waals kraft; derfor er det flydende ved stuetemperatur. Det krævede stadig meget lav energi for at eliminere H-bindingsenergien sammenlignet med ionbindingerne. Derfor er dens smeltepunkt er forholdsvis nederste.
Er vand dipol dipol?
Vand har en stærk brintbinding dipol - dipol intermolekylære kræfter, der giver vand en høj overfladespænding og en høj fordampningsvarme, og det gør det til et stærkt opløsningsmiddel.
Anbefalede:
Hvilket ikke-metal har højt smelte- og kogepunkt?

Diamant er en allotrop/form for kulstof. Så kulstof (i form af diamant) er det eneste ikke-metal, som har et meget højt smeltepunkt
Hvorfor ionisk forbindelse har højt smelte- og kogepunkt?

Ioniske forbindelser har høje smelte- og kogepunkter, fordi der er en stærk elektrostatisk tiltrækningskraft mellem de modsat ladede ioner, og der kræves derfor en stor mængde energi for at bryde den stærke bindingskraft mellem ioner
Har natrium et højt smeltepunkt?

97,79 °C
Hvorfor har vand et højt smeltepunkt?
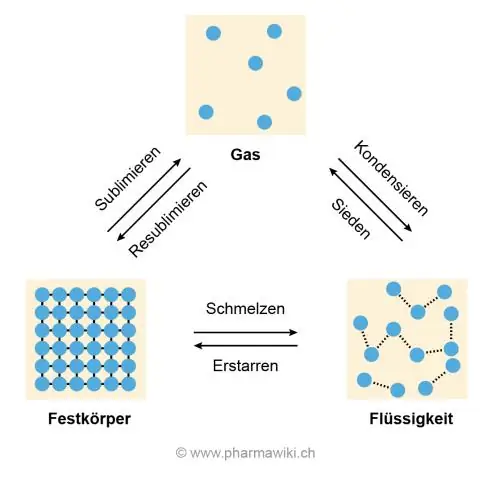
Årsagen til de høje smelte- og kogetemperaturer er hydrogenbindingen mellem vandmolekyler, der får dem til at klæbe sammen og modstå at blive trukket fra hinanden, hvilket er det, der sker, når is smelter og vand koger til en gas
Hvorfor har natrium et højt smeltepunkt?

Natriumchlorid har et højt smeltepunkt på grund af den stærke elektrostatiske tiltrækning mellem dets positive og negative ioner; dette kræver mere varmeenergi at overvinde. Den har også en gigantisk gitterstruktur, hvilket betyder, at den indeholder millioner af stærke ionbindinger
