
Video: Hvordan er emissionsspektre bevis for elektronskaller i Bohr-modellen?
2024 Forfatter: Miles Stephen | [email protected]. Sidst ændret: 2023-12-15 23:34
Tilstedeværelsen af kun visse linjer i atomare spektre mente at en elektron kan kun vedtage bestemte diskrete energiniveauer (energien er kvantificeret); deraf ideen om kvante skaller . Fotonfrekvenserne absorberet eller udsendes af et atom er fikseret af forskellene mellem energiniveauerne i banerne.
Hvad angår dette, hvordan redegjorde Bohr-modellen for atomernes emissionsspektre?
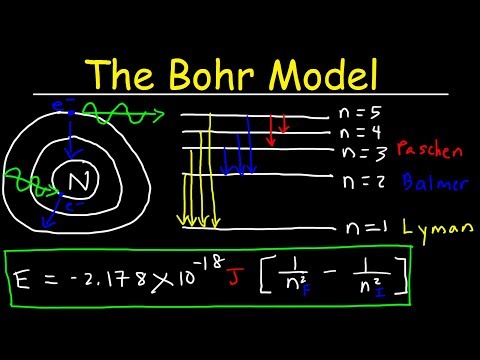
Bohrs model af brinten atom gav en nøjagtig forklaring på dets observerede emissionsspektrum . Elektroner kan bevæge sig fra en bane til en anden ved at absorbere eller udsende energi, hvilket giver anledning til karakteristika spektre.
hvilke beviser understøtter Bohr-modellen? Bohr model og Atomic Spectra The beviser plejede understøtte Bohr-modellen kom fra atomspektrene. Bohr antydet, at et atomspektrum skabes, når elektronerne i et atom bevæger sig mellem energiniveauer.
Med hensyn til dette, hvilke beviser er der for elektroner i skaller?
Ioniseringsenergi – beviset til skaller og under- skaller Ioniseringsenergi er - en mål på det mængden af energi, der skal til for at fjerne elektroner fra atomer. Som elektroner er negativt ladede og protoner ind det kerne er positivt ladede, der vil være en attraktion mellem dem.
Hvordan finder du emissionsspektret?
Frekvenserne af lys, som et atom kan udsende, er afhængige af tilstande, elektronerne kan være i. Når den exciteres, bevæger en elektron sig til et højere energiniveau eller orbital. Når elektronen falder tilbage til sit jordniveau, er lyset udsendes.
Anbefalede:
Hvad er de forskellige kilder til bevis for evolution?

Beviser for evolution kommer fra mange forskellige områder af biologien: Anatomi. Arter kan dele lignende fysiske træk, fordi træk var til stede i en fælles forfader (homologe strukturer). Molekylær Biologi. DNA og den genetiske kode afspejler livets fælles herkomst. Biogeografi. Fossiler. Direkte observation
Hvordan er embryologi bevis for evolution?

Studiet af en type bevis for evolution kaldes embryologi, studiet af embryoner. Mange træk af en type dyr optræder i embryonet af en anden type dyr. For eksempel har fiskeembryoner og menneskelige embryoner begge gællespalter. Hos fisk udvikler de sig til gæller, men hos mennesker forsvinder de før fødslen
Hvordan giver komparativ embryologi bevis for evolution?

Evidens for evolution: Sammenlignende embryologi er en af de vigtigste beviser til støtte for evolution. I komparativ embryologi sammenlignes anatomien af embryoner fra forskellige arter gennem embryonernes udvikling. Ligheder mellem forskellige arter indikerer, at vi alle kom fra en fælles forfader
Hvilket grundstof har det samme antal elektronskaller som calcium?

Ja, calcium er defineret som et metal på grund af både dets fysiske og kemiske egenskaber. De har alle en ydre skal med to elektroner og er meget reaktive. Disse elementer i den anden kolonne har to elektroner klar til at lave forbindelser. Det burde ikke overraske dig, at calcium har en valens på 2
Hvordan er emissionsspektre beviser for elektronskaller?

Tilstedeværelsen af kun bestemte linjer i atomspektre betød, at en elektron kun kan adoptere bestemte diskrete energiniveauer (energien er kvantiseret); deraf ideen om kvanteskaller. De fotonfrekvenser, der absorberes eller udsendes af et atom, er fastsat af forskellene mellem energiniveauerne i kredsløbene
