Indholdsfortegnelse:

Video: Hvad er det matematiske forhold mellem frysepunktsdepression og molalitet?

2024 Forfatter: Miles Stephen | [email protected]. Sidst ændret: 2023-12-15 23:34
Frysepunktsdepression er en kolligativ egenskab, der observeres i opløsninger, der er resultatet af introduktion af opløste molekyler til et opløsningsmiddel. Frysepunkterne for opløsninger er alle lavere end for det rene opløsningsmiddel og er direkte proportionale med molaliteten af det opløste stof.
Tilsvarende, hvordan beregner man Molalitet ud fra frysepunktsdepression?
Strategi:
- Trin 1: Beregn frysepunktsnedsættelsen af benzen. Tf = (Frysepunkt for rent opløsningsmiddel) - (Frysepunkt for opløsning)
- Trin 2: Beregn molkoncentrationen af opløsningen. molalitet = mol opløst stof / kg opløsningsmiddel.
- Trin 3: Beregn Kf af løsningen. Tf = (Kf) (m)
Ligeledes, hvorfor bruges Molality i frysepunktet? Wendy K. Kolligative egenskaber er fysiske egenskaber ved opløsninger, såsom kogning punkt højde og frysepunkt depression. Det er derfor, vi bruger molalitet (mol opløst stof pr. kg opløsningsmiddel), da kg opløsningsmiddel ikke ændres med temperatur.
Spørgsmålet er også, hvad mener du med nedsættelse af frysepunktet?
Frysepunktsdepression opstår, når frysepunkt af en væske sænkes eller deprimeret ved at tilføje en anden forbindelse til den. Løsningen har en lavere frysepunkt end det rene opløsningsmiddel.
Hvordan påvirker molalitet kogepunktet?
Jo højere koncentration ( molalitet ), jo højere kogepunkt . Du kan tænke på dette effekt som opløst opløst stof, der fortrænger opløsningsmiddelmolekyler ved overfladen, hvor kogende opstår. Derfor kræver det en højere temperatur for nok opløsningsmiddelmolekyler til at undslippe for at fortsætte kogende ved atmosfærisk tryk.
Anbefalede:
Hvad er det matematiske forhold mellem strømmodstand og spændingsdims?
Ohms lov. Forholdet mellem spænding, strøm og modstand er beskrevet af Ohms lov. Denne ligning, i = v/r, fortæller os, at strømmen, i, der strømmer gennem et kredsløb, er direkte proportional med spændingen, v, og omvendt proportional med modstanden, r
Hvad er et forhold mellem linjer og cirkler?

En linje kan have tre typer relationer til en cirkel… (1) En linje kan skære en cirkel i to forskellige punkter på dens omkreds. Sådan en linje kaldes en Secant. (2) En linje må kun berøre en cirkel i et punkt på dens omkreds
Hvad er det skiftende forhold mellem volumen og overfladeareal, når et objekt bliver større?
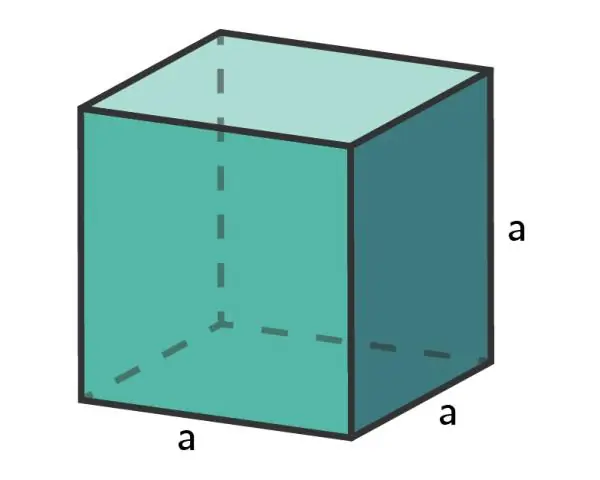
Når terningstørrelsen øges, eller cellen bliver større, falder forholdet mellem overfladeareal og volumen - SA:V-forhold. Når en genstand/celle er meget lille, har den et stort forhold mellem overfladeareal og volumen, mens en stor genstand/celle har et lille forhold mellem overfladeareal og volumen
Hvad er det symbiotiske forhold mellem Euprymna bobtail blæksprutte og bioluminescerende bakterier?

Bobtail-blæksprutter har et symbiotisk forhold til selvlysende bakterier (Aliivibrio fischeri), som lever i et særligt lysorgan i blækspruttens kappe. Bakteriernes luminescerende egenskaber regulerer genekspression i lysorganet
Hvordan påvirker frysepunktsdepression molekylvægten?

Når molmassen stiger, falder frysepunktsnedsættelsen således. Det vil sige, at forøgelse af den molære (eller molekylære) masse vil have en mindre effekt på frysepunktet
