Indholdsfortegnelse:

Video: Hvordan løser man for reaktionsvarme?

2024 Forfatter: Miles Stephen | [email protected]. Sidst ændret: 2024-01-18 08:14
Entalpi af opløsning (opløsningsvarme) Eksempel
- Beregn det varme frigivet, q, i joule (J), af reaktion : q = masse(vand) × specifik varme kapacitet(vand) × ændring i temperatur( løsning )
- Beregn mol af opløst stof (NaOH(s)): mol = masse ÷ molær masse.
- Beregn det entalpi ændring, ΔH, i kJ mol-1 af opløst stof:
Ligeledes, hvordan finder du dannelsesvarmen?
Denne ligning angiver i det væsentlige, at standarden entalpi ændring af dannelse er lig med summen af standardentalpierne af dannelse af produkterne minus summen af standardentalpierne af dannelse af reaktanterne. og standarden dannelsesentalpi værdier: ΔH fo[A] = 433 KJ/mol. ΔH fo[B] = -256 KJ/mol.
Efterfølgende er spørgsmålet, hvad betyder opløsningsvarme? Definition af opløsningens varme .: det varme udvikles eller absorberes, når et stof opløses specifikt: den involverede mængde, når en mol eller nogle gange et gram opløses i et stort overskud af opløsningsmiddel.
Ved også, hvordan man beregner ændring i varme?
Hvornår varme overførsel er involveret, brug denne formel: lave om i temperatur = Q / cm til Beregn det lave om i temperatur fra en bestemt mængde af varme tilføjet. Q repræsenterer varme tilføjet, c er det specifikke varme kapaciteten af det stof, du opvarmer, og m er massen af det stof, du opvarmer.
Hvad betyder forbrændingsvarme?
Forbrændingsvarme (ΔH°c) er mål for mængden af frigivet energi i form af varme (q) når en mol af et stof forbrændes ( forbrænding ). Produktionen af varme betyder, at reaktionen er en eksoterm proces og afgiver energi.
Anbefalede:
Hvordan løser man en andengradsligning ved hjælp af nulfaktorloven?

Af dette kan vi udlede, at: Hvis produktet af to vilkårlige tal er nul, så er det ene eller begge tal nul. Det vil sige, hvis ab = 0, så er a = 0 eller b = 0 (hvilket inkluderer muligheden for, at a = b = 0). Dette kaldes nulfaktorloven; og vi bruger det ofte til at løse andengradsligninger
Hvordan løser man ideel gaslov?

Ideal Gas Lov Formel Spørgsmål til Ideal Gas Lov Formel: Svar: Volumenet er V = 890,0mL og temperaturen er T = 21°C og trykket er P = 750mmHg. PV = nRT. Svar: Antallet af mol er n = 3,00 mol, temperaturen er T = 24°C og trykket er P = 762,4 mmHg. PV = nRT
Hvordan løser man totrinsligninger i præalgebra?

VIDEO På samme måde, hvad er de 4 trin til at løse en ligning? En 4-trins guide til løsning af ligninger (del 2) Trin 1: Forenkle hver side af ligningen. Som vi lærte sidst, er det første skridt i løsningen af en ligning at gøre ligningen så enkel som muligt.
Hvordan løser man gange og dividere brøker?
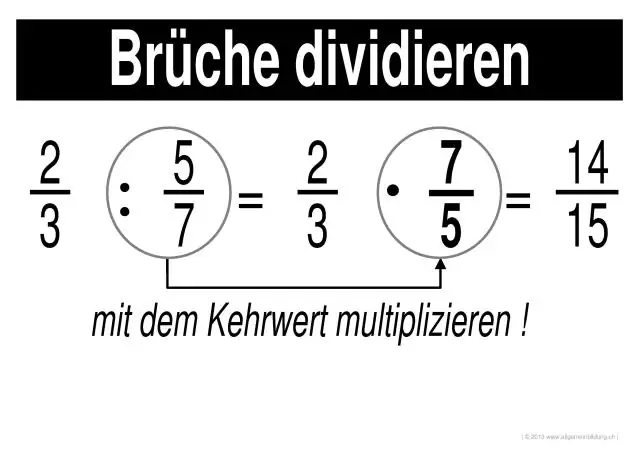
Gang og dividere brøker Trin 1: Gang tællere fra hver brøk med hinanden (tallene øverst). Resultatet er tælleren for svaret. Trin 2: Gang nævnerne for hver brøk med hinanden (tallene i bunden). Resultatet er nævneren for svaret. Trin 3: Forenkle eller reducere svaret
Hvordan hænger temperatur og reaktionsvarme sammen?

Reaktionsvarme, mængden af varme, der skal tilsættes eller fjernes under en kemisk reaktion for at holde alle tilstedeværende stoffer ved samme temperatur. Hvis reaktionsvarmen er positiv, siges reaktionen at være endoterm; hvis negativ, eksoterm
